N新华 科技日报 参考消息
广州日报央广网 新京报
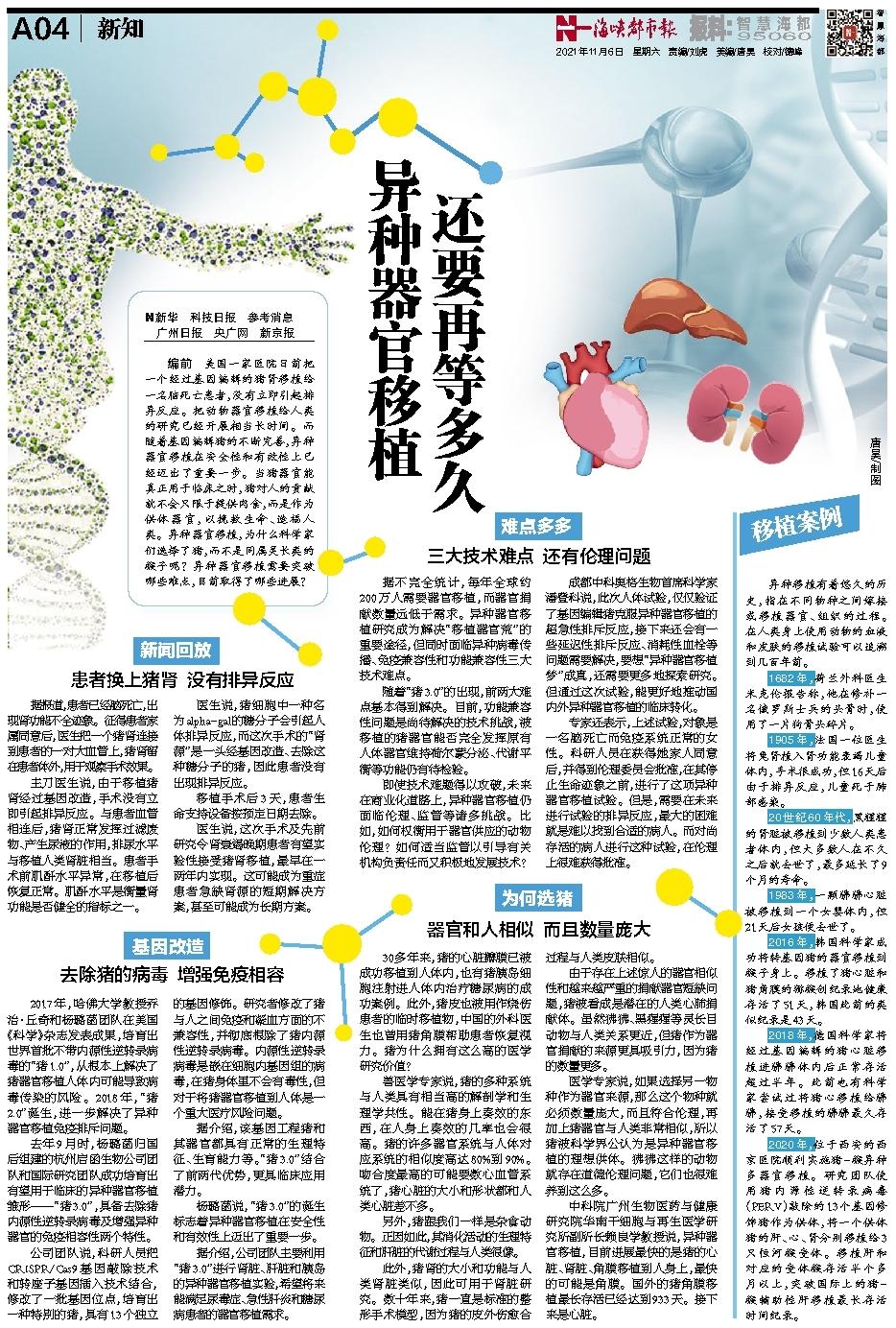
编前 美国一家医院日前把一个经过基因编辑的猪肾移植给一名脑死亡患者,没有立即引起排异反应。把动物器官移植给人类的研究已经开展相当长时间。而随着基因编辑猪的不断完善,异种器官移植在安全性和有效性上已经迈出了重要一步。当猪器官能真正用于临床之时,猪对人的贡献就不会只限于提供肉食,而是作为供体器官,以挽救生命、造福人类。异种器官移植,为什么科学家们选择了猪,而不是同属灵长类的猴子呢?异种器官移植需要突破哪些难点,目前取得了哪些进展?
新闻回放患者换上猪肾没有排异反应
据报道,患者已经脑死亡,出现肾功能不全迹象。征得患者家属同意后,医生把一个猪肾连接到患者的一对大血管上,猪肾留在患者体外,用于观察手术效果。
主刀医生说,由于移植猪肾经过基因改造,手术没有立即引起排异反应。与患者血管相连后,猪肾正常发挥过滤废物、产生尿液的作用,排尿水平与移植人类肾脏相当。患者手术前肌酐水平异常,在移植后恢复正常。肌酐水平是衡量肾功能是否健全的指标之一。
医生说,猪细胞中一种名为alpha-gal的糖分子会引起人体排异反应,而这次手术的“肾源”是一头经基因改造、去除这种糖分子的猪,因此患者没有出现排异反应。
移植手术后3天,患者生命支持设备按预定日期去除。
医生说,这次手术及先前研究令肾衰竭晚期患者有望实验性接受猪肾移植,最早在一两年内实现。这可能成为重症患者急缺肾源的短期解决方案,甚至可能成为长期方案。
基因改造去除猪的病毒增强免疫相容
2017年,哈佛大学教授乔治·丘奇和杨璐菡团队在美国《科学》杂志发表成果,培育出世界首批不带内源性逆转录病毒的“猪1.0”,从根本上解决了猪器官移植人体内可能导致病毒传染的风险。2018年,“猪2.0”诞生,进一步解决了异种器官移植免疫排斥问题。
去年9月时,杨璐菡归国后组建的杭州启函生物公司团队和国际研究团队成功培育出有望用于临床的异种器官移植雏形——“猪3.0”,具备去除猪内源性逆转录病毒及增强异种器官的免疫相容性两个特性。
公司团队说,科研人员把CRISPR/Cas9基因敲除技术和转座子基因插入技术结合,修改了一批基因位点,培育出一种特别的猪,具有13个独立
的基因修饰。研究者修改了猪与人之间免疫和凝血方面的不兼容性,并彻底根除了猪内源性逆转录病毒。内源性逆转录病毒是嵌在细胞内基因组的病毒,在猪身体里不会有毒性,但对于将猪器官移植到人体是一个重大医疗风险问题。
据介绍,该基因工程猪和其器官都具有正常的生理特征、生育能力等。“猪3.0”结合了前两代优势,更具临床应用潜力。
杨璐菡说,“猪3.0”的诞生标志着异种器官移植在安全性和有效性上迈出了重要一步。
据介绍,公司团队主要利用“猪3.0”进行肾脏、肝脏和胰岛的异种器官移植实验,希望将来能满足尿毒症、急性肝炎和糖尿病患者的器官移植需求。
难点多多三大技术难点还有伦理问题
据不完全统计,每年全球约200万人需要器官移植,而器官捐献数量远低于需求。异种器官移植研究成为解决“移植器官荒”的重要途径,但同时面临异种病毒传播、免疫兼容性和功能兼容性三大技术难点。
随着“猪3.0”的出现,前两大难点基本得到解决。目前,功能兼容性问题是尚待解决的技术挑战,被移植的猪器官能否完全发挥原有人体器官维持荷尔蒙分泌、代谢平衡等功能仍有待检验。
即使技术难题得以攻破,未来在商业化道路上,异种器官移植仍面临伦理、监管等诸多挑战。比如,如何权衡用于器官供应的动物伦理?如何适当监管以引导有关机构负责任而又积极地发展技术?
成都中科奥格生物首席科学家潘登科说,此次人体试验,仅仅验证了基因编辑猪克服异种器官移植的超急性排斥反应,接下来还会有一些延迟性排斥反应、消耗性血栓等问题需要解决,要想“异种器官移植梦”成真,还需要更多地探索研究。但通过这次试验,能更好地推动国内外异种器官移植的临床转化。
专家还表示,上述试验,对象是一名脑死亡而免疫系统正常的女性。科研人员在获得她家人同意后,并得到伦理委员会批准,在其停止生命迹象之前,进行了这项异种器官移植试验。但是,需要在未来进行试验的排异反应,最大的困难就是难以找到合适的病人。而对尚存活的病人进行这种试验,在伦理上很难获得批准。
为何选猪器官和人相似而且数量庞大
30多年来,猪的心脏瓣膜已被成功移植到人体内,也有猪胰岛细胞注射进人体内治疗糖尿病的成功案例。此外,猪皮也被用作烧伤患者的临时移植物,中国的外科医生也曾用猪角膜帮助患者恢复视力。猪为什么拥有这么高的医学研究价值?
兽医学专家说,猪的多种系统与人类具有相当高的解剖学和生理学共性。能在猪身上奏效的东西,在人身上奏效的几率也会很高。猪的许多器官系统与人体对应系统的相似度高达80%到90%。吻合度最高的可能要数心血管系统了,猪心脏的大小和形状都和人类心脏差不多。
另外,猪跟我们一样是杂食动物。正因如此,其消化活动的生理特征和肝脏的代谢过程与人类很像。
此外,猪肾的大小和功能与人类肾脏类似,因此可用于肾脏研究。数十年来,猪一直是标准的整形手术模型,因为猪的皮外伤愈合
过程与人类皮肤相似。
由于存在上述惊人的器官相似性和越来越严重的捐献器官短缺问题,猪被看成是潜在的人类心肺捐献体。虽然狒狒、黑猩猩等灵长目动物与人类关系更近,但猪作为器官捐献的来源更具吸引力,因为猪的数量更多。
医学专家说,如果选择另一物种作为器官来源,那么这个物种就必须数量庞大,而且符合伦理,再加上猪器官与人类非常相似,所以猪被科学界公认为是异种器官移植的理想供体。狒狒这样的动物就存在道德伦理问题,它们也很难养到这么多。
中科院广州生物医药与健康研究院华南干细胞与再生医学研究所副所长赖良学教授说,异种器官移植,目前进展最快的是猪的心脏、肾脏、角膜移植到人身上,最快的可能是角膜。国外的猪角膜移植最长存活已经达到933天。接下来是心脏。
移植案例
异种移植有着悠久的历史,指在不同物种之间嫁接或移植器官、组织的过程。在人类身上使用动物的血液和皮肤的移植试验可以追溯到几百年前。
1682年,荷兰外科医生米克伦报告称,他在修补一名俄罗斯士兵的头骨时,使用了一片狗骨头碎片。
1905年,法国一位医生将兔肾植入肾功能衰竭儿童体内,手术很成功,但16天后由于排异反应,儿童死于肺部感染。
20世纪60年代,黑猩猩的肾脏被移植到少数人类患者体内,但大多数人在不久之后就去世了,最多延长了9个月的寿命。
1983年,一颗狒狒心脏被移植到一个女婴体内,但21天后女孩便去世了。
2016年,韩国科学家成功将转基因猪的器官移植到猴子身上。移植了猪心脏和猪角膜的猕猴创纪录地健康存活了51天,韩国此前的类似纪录是43天。
2018年,德国科学家将经过基因编辑的猪心脏移植进狒狒体内后正常存活超过半年。此前也有科学家尝试过将猪心移植给狒狒,接受移植的狒狒最久存活了57天。
2020年,位于西安的西京医院顺利实施猪-猴异种多器官移植。研究团队使用猪内源性逆转录病毒(PERV)敲除的13个基因修饰猪作为供体,将一个供体猪的肝、心、肾分别移植给3只恒河猴受体。移植肝和对应的受体猴存活半个多月以上,突破国际上的猪-猴辅助性肝移植最长存活时间纪录。